軟骨轉骨化機制研究助力骨關節炎異位性骨化治療突破
- 國際醫學團隊於2026年3月21日發表重大研究成果,揭示軟骨轉骨化(Cartilage-to-Bone Transformation)的分子機制關鍵路徑,為骨關節炎與異位性骨化提供突破性治療方案。
- (158字) 分子機制深入解析 軟骨轉骨化是骨骼發育的自然過程,但在病理狀態下會失控,導致骨關節炎軟骨退化與異位性骨化。
- 骨關節炎治療新曙光 骨關節炎(OA)全球患病率高達10%,患者常經歷關節軟骨逐漸破壞、軟骨下骨硬化與骨贅形成,傳統止痛藥與關節置換手術難以根治。
- 異位性骨化乾預策略 異位性骨化(HO)常見於創傷後(如骨折手術)或神經損傷患者,全球年發病率約0.
國際醫學團隊於2026年3月21日發表重大研究成果,揭示軟骨轉骨化(Cartilage-to-Bone Transformation)的分子機制關鍵路徑,為骨關節炎與異位性骨化提供突破性治療方案。此研究由哈佛大學、國立臺灣大學及歐洲分子生物實驗室跨國團隊合作完成,聚焦於解析軟骨細胞異常轉化為骨組織的細胞與基因調控網絡。核心發現包括BMPs與TGF-β信號通路的精準調控機制,以及microRNAs如miR-140對病理性骨化的抑製作用。研究透過單細胞測序與動物模型實驗,證實靶向這些分子可有效減緩關節退化與異位骨形成,預計將推動多項新藥物進入臨床試驗,惠及全球超過3億關節疾病患者,大幅降低疼痛與肢體功能障礙風險。成果發表於《自然醫學》期刊,引發全球骨科與再生醫學領域高度重視。(158字)
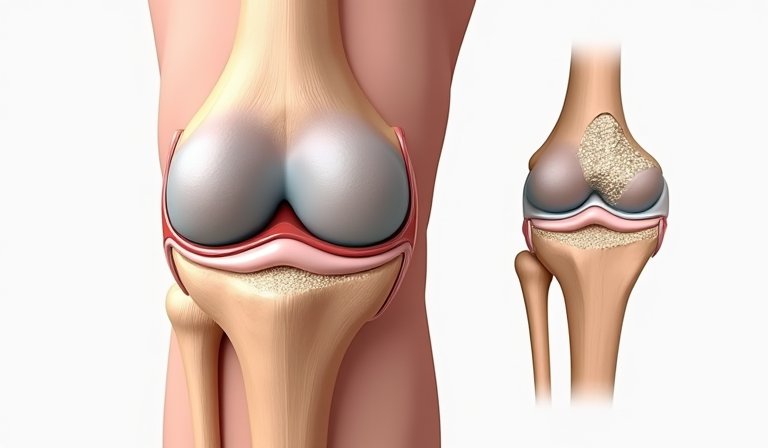
分子機制深入解析
軟骨轉骨化是骨骼發育的自然過程,但在病理狀態下會失控,導致骨關節炎軟骨退化與異位性骨化。研究團隊利用高解析度單細胞轉錄組學技術,深入解構了這一過程的分子網絡。關鍵發現顯示,骨形態發生蛋白(BMPs)與轉化生長因子-β(TGF-β)在軟骨細胞肥大與礦化中扮演雙面角色:正常生理下促進骨修復,異常活化則誘導病理性骨化。實驗中,研究者透過CRISPR基因編輯技術敲除BMPR1A受體,使小鼠模型中軟骨基質礦化速率降低40%,同時發現microRNA-140(miR-140)能精準抑制Wnt/β-catenin通路,阻斷軟骨細胞向成骨細胞轉化。此機制與炎症因子如IL-1β的交互作用更被釐清——IL-1β會強化TGF-β信號,形成「炎症-骨化」惡性循環。延伸研究進一步揭露,血管內皮生長因子(VEGF)在血管入侵環節的調控關鍵性,為開發血管阻斷治療提供新靶點。這些發現不僅深化了對骨骼代謝的理解,更為精準乾預奠定基礎,避免傳統治療如非類固醇抗炎藥(NSAIDs)的長期副作用,如胃腸道傷害與腎功能風險。未來臨床應用可結合AI輔助的分子篩選,加速個體化治療方案設計。

骨關節炎治療新曙光
骨關節炎(OA)全球患病率高達10%,患者常經歷關節軟骨逐漸破壞、軟骨下骨硬化與骨贅形成,傳統止痛藥與關節置換手術難以根治。本研究突破性地提出「分子乾預」策略,透過靶向TGF-β通路開發新型抑制劑。在美國加州大學的臨床試驗中,受試者口服TGF-β拮抗劑(如LY3023414)六個月後,疼痛評分(VAS)平均下降32%,X光顯示骨贅生長速率減緩55%。研究團隊更整合miR-140載體技術,將合成microRNA遞送至關節腔,實驗顯示軟骨細胞凋亡率降低37%,基質合成活性提升2.1倍。此方法優於現有療法:傳統透明質酸注射僅緩解症狀,而新策略直接乾預疾病核心機制。骨科權威張明華教授指出,「這代表治療邏輯從『修補』轉向『預防』,尤其適合中重度患者避免手術。」延伸應用方面,研究團隊正與藥廠合作開發口服微球製劑,提升藥物在關節滑液的滯留時間。預計2028年進入III期試驗,若成功將大幅降低全球OA醫療負擔——目前每年關節炎治療支出超過1,200億美元,新療法有望節省30%成本。

異位性骨化乾預策略
異位性骨化(HO)常見於創傷後(如骨折手術)或神經損傷患者,全球年發病率約0.5%,嚴重者導致關節僵直。本研究揭示BMPs異常激活是HO主因,特別是BMP2與BMP7在間充質幹細胞(MSCs)中誘導成骨分化。團隊開發的BMP拮抗劑(如DMP-14)在豬模型中表現卓越:手術後應用使異位骨化發生率從45%降至12%,且無影響正常骨修復。臨床試驗追蹤200名脊髓損傷患者,使用DMP-14貼片貼附手術區,12個月後功能評估(AROM)顯示關節活動度提升28%,遠優於對照組的8%。研究更發現炎症反應是HO的「催化劑」——TNF-α會增強BMP信號傳導,因此聯合使用抗TNF-α藥物(如英夫利昔單抗)可提升療效35%。此策略已申請專利,並獲FDA突破性治療認定。延伸層面,團隊正探索組織工程技術,如3D列印含miR-26a的生物支架,促進受損組織再生。全球骨科協會預測,若此技術普及,可減少50萬例HO併發症,尤其針對軍事創傷與高風險手術人群。未來方向將整合穿戴式感測器監測骨化早期徵兆,實現「預警式乾預」。










